INDICE
- Cenni storici
- Atomi e molecole
- Isotopi e ioni
- Radioattività e fissione
- Quark
- Snark e Boojum
- Materia e fasi di aggregazione
- Antimateria
- Materia ed energia oscura
- Tavola Periodica degli elementi
1. CENNI STORICI
"Siamo polvere di stelle"
Carl Sagan
La Chimica (una parola che si fa risalire all'antico egizio Kemà) è la scienza che studia la composizione della materia e come questa si comporta.
Anticamente, esistevano due teorie sulla natura della materia, entrambe figlie del pensiero filosofico greco: la teoria di Democrito, detta "Atomica" perché postulava che ogni cosa fosse costituita da corpuscoli indivisibili (a-tomos, non-divisibile, in greco antico), e la teoria di Aristotele, detta "Elementale" perché postulava che ogni oggetto fisico fosse costituito da una combinazione variabile di quattro elementi: Aria, Acqua, Fuoco e Terra (nel Wu Xing, la Teoria dei Cinque Elementi di origine cinese, gli elementi costitutivi sono invece Legno, Fuoco, Terra, Metallo e Acqua).
Durante il Medioevo, in Europa (ma le radici si ritrovano già tra il II e il V secolo, in Egitto), la forza della filosofia aristotelica ha portato all'abbandono della teoria atomica e alla nascita dell'Alchimia, intesa come mezzo e metodo per comprendere l'operato dei Quattro Elementi nella vita dell'uomo e come strumento per modificare la natura. In ambito alchemico, è particolarmente nota la ricerca della "Pietra Filosofale", uno strumento che sarebbe stato in grado tanto di trasformare il piombo (o altri metalli: anche tutti, secondo le varie versioni) in oro, quanto di donare l'immortalità.
Durante l'Illuminismo, o Secolo dei Lumi, le teorie alchemiche vengono progressivamente abbandonate a favore di un approccio scientifico e razionale allo studio della chimica. Nel 1661 il chimico irlandese Robert Boyle pubblica un testo ("The Sceptical Chymist / Il Chimico scettico") in cui, per la prima volta, si parla di elementi e di composti chimici.
Studi ed esperimenti di laboratorio dimostrano l'esistenza di una molteplicità di elementi, che vengono ordinati nel 1869 dal fisico russo Mendeleev nella famosa "Tavola Periodica degli Elementi". Nel 1937, infine, il fisico italiano Emilio Segrè sintetizza il "Tecnezio", il primo elemento chimico creato artificialmente, aprendo alla chimica una nuova strada che la porterà anche a diventare ciò che oggi conosciamo come "fisica".

2. ATOMI E MOLECOLE
La chimica moderna è considerata una "scienza centrale", perché è alla base di molte altre discipline scientifiche fra cui l'astronomia, la fisica, la scienza dei materiali, la biologia e la geologia.
La chimica moderna riprende il concetto di Democrito di "atomo" quale mattone ultimo che costituisce la materia. Già alla fine del XIX secolo, però, la scoperta dell'esistenza dell'elettrone ha dimostrato che l'atomo può in realtà essere a sua volta suddiviso in tre componenti: Protone, Neutrone ed Elettrone.
Il Protone è un componente del nucleo di ogni atomo. È una particella con carica elettrica positiva, e il numero di protoni presenti nel nucleo atomico è ciò che distingue un elemento chimico da un altro: se nel nucleo c'è un solo protone è Idrogeno, se ce ne sono due è Elio, se ce ne sono tre è Litio e così via.
Il Neutrone è una particella, con carica elettrica nulla, presente in numero variabile nel nucleo di ogni atomo (ad eccezione del Prozio, il più comune isotopo dell'Idrogeno, il cui nucleo è composto solo da un protone).
L'Elettrone è una particella con carica elettrica negativa. È l'unica delle tre particelle non presente nel nucleo dell'atomo (secondo la rappresentazione classica degli atomi, gli elettroni ruotano attorno al nucleo come pianeti attorno ad una stella). Un diverso numero di elettroni in un atomo dà origine agli ioni di quell'elemento.
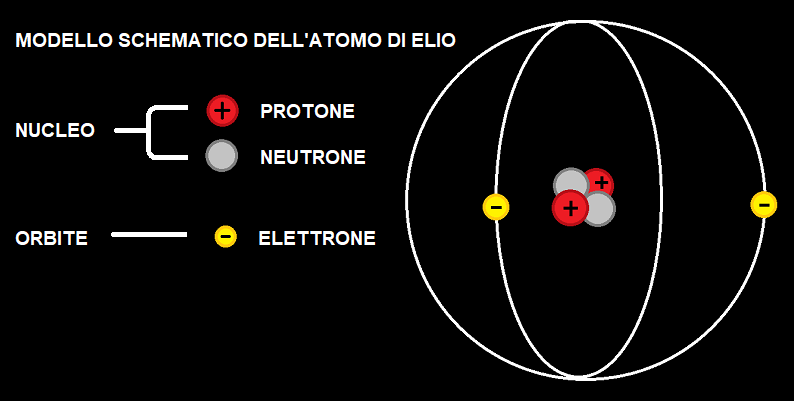
Il numero di protoni presenti nel nucleo di un atomo non cambia: la differenza di questo valore, infatti, è ciò che distingue un elemento da un altro nella Tavola Periodica degli elementi, ideata dal fisico russo Mendeleev.
Il numero di protoni presenti nel nucleo di un atomo viene indicato con il Numero Atomico (Z, dal tedesco Zahl, che significa appunto "numero").
Poiché la carica elettrica di un atomo è sempre nulla, e i protoni hanno carica positiva, questo numero indica anche - indirettamente - il numero di elettroni presenti nello stesso atomo.
Ogni protone, neutrone o elettrone ha una specifica massa, che non varia.
Dalla massa del nucleo di un elemento, considerando che il numero di protoni è definito dal suo numero atomico, è possibile ricavare la massa, e quindi il numero, di neutroni presenti.
Il valore della massa di un nucleo (dato dalla somma della massa dei neutroni e dei protoni), detto Numero di massa, è ciò che consente di distinguere un isotopo di un elemento da un altro isotopo dello stesso elemento.
Nel 2019, 150 anni dopo l'introduzione della Tavola Periodica da parte del fisico russo Mendeleev, questa comprende 118 elementi: i primi 98 sono considerati "naturali", cioè esistenti in natura (anche se gli elementi dal 93 al 98 si trovano solo in tracce), mentre gli altri sono "sintetici", cioè esistono solo in condizioni di laboratorio, sono altamente instabili e tendono a decadere - trasformandosi in elementi più semplici e stabili - in pochi istanti.
Anche fra gli elementi naturali alcuni sono stabili (come il Ferro), mentre altri sono instabili (come l'Uranio e tutti gli elementi radioattivi), sebbene su scala temporale abbastanza lunga da consentirgli di esistere in natura.
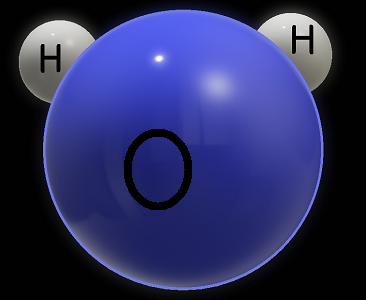
In natura, gli atomi possono trovarsi sia isolati sia in forma di Molecola, un insieme elettricamente neutro composto da due o più atomi di uno stesso elemento o di elementi diversi, uniti da un legame chimico. La più nota delle molecole è l'acqua, la cui formula chimica è H2O, ovvero due atomi di Idrogeno uniti ad un atomo di Ossigeno.

3. ISOTOPI E IONI
Isotopo e Ione sono termini usati per indicare atomi che hanno una struttura diversa dall'elemento base.
Il termine Isotopo indica un atomo il cui nucleo ha un identico numero di protoni rispetto all'elemento base, ma un differente numero di neutroni (ha quindi lo stesso Numero Atomico ma un differente Numero di massa).
Poiché i neutroni hanno carica elettrica nulla, le proprietà chimiche dell'atomo non variano mentre cambiano - anche in modo sostanziale - le sue proprietà fisiche.
I più noti Isotopi sono quelli dell'Idrogeno: Prozio, Deuterio e Trizio.
Il Prozio è la più comune forma in cui sia possibile trovare un atomo di idrogeno: un nucleo composto da un solo protone, con un elettrone a bilanciarne la carica elettrica.
Questo isotopo è talmente comune e abbondante che, per semplicità, non viene mai nominato: ci si riferisce semplicemente all'Idrogeno (simbolo chimico: H), sottintendendo che si stia parlando di questo isotopo.
Il Deuterio è il secondo più abbondante isotopo dell'Idrogeno: differisce dal Prozio per la presenza, nel nucleo, di un neutrone.
Il Deuterio, sebbene poco abbondante in natura, è talmente rilevante da aver ricevuto una sua lettera identificativa, "onore" di solito riservato agli elementi chimici: così, oltre che con le più corrette formule 2H o H-2, viene spesso indicato con la lettera D.
Il Trizio è il terzo più abbondante isotopo dell'Idrogeno, e differisce dal Prozio per la presenza, nel nucleo, di due neutroni.
Come il Deuterio, anche il Trizio ha ricevuto una sua lettera identificativa: così, lo si può trovare indicato con le formule 3H o H-3 o con la lettera T.
Il termine Ione indica un atomo con un numero di elettroni diverso rispetto all'elemento base.
Poiché gli elettroni hanno carica elettrica negativa, variare il loro numero rispetto a quello dei protoni genera uno squilibrio elettrico nell'intero atomo.
Un eccesso di elettroni, aumentando la carica negativa rispetto a quella positiva, origina uno Ione Negativo (chiamato anche Anione). Al contrario, una carenza di elettroni aumenta la carica positiva e origina uno Ione Positivo (chiamato anche Catione).
Poiché lo stato naturale di un atomo è la carica elettrica nulla, gli ioni sono per loro natura instabili: gli atomi tendono quindi al riequilibrio energetico, perdendo gli elettroni in eccesso o acquisendo elettroni liberi.

4. RADIOATTIVITÀ E FISSIONE
All'interno di un nucleo atomico agiscono due forze contrapposte: l'interazione nucleare forte, che lega tra di loro i Nucleoni (protoni e neutroni) e la repulsione elettrostatica, che costringe i protoni a respingersi reciprocamente perché hanno cariche dello stesso segno. Siccome la repulsione ha raggio d'azione infinito, pur decrescendo d'intensità al crescere del quadrato della distanza, mentre la forza nucleare forte ha raggio d'azione pari a circa un diametro protonico, i protoni possono legare a sé solo quelli più vicini, mentre subiscono la repulsione di tutti gli altri, anche dei più lontani.
Se il nucleo è piccolo non sorgono problemi, ma se diventa troppo grande la repulsione dei protoni lontani predomina sull'attrazione di quelli vicini, e il nucleo diventa instabile.
Per mantenere la propria stabilità, il nucleo di un atomo ha due possibilità: aumentare il numero di neutroni o emettere protoni.
I neutroni sono Nucleoni, particelle cioè che - insieme ai protoni - compongono il nucleo di un atomo. I neutroni hanno una massa molto simile a quella dei protoni, e quindi contribuiscono come loro all'interazione nucleare forte, ma hanno carica elettrica nulla, e quindi non partecipano alla repulsione elettrostatica. In più, frapponendosi fra i protoni e aumentando la distanza fra loro, ne diminuiscono gli effetti.
Al di sopra di una certa soglia, comunque, nemmeno la presenza dei neutroni è più in grado di assicurare stabilità al nucleo atomico, che riguadagna equilibrio liberandosi dei protoni in eccesso.
Questo processo, chiamato Fissione Spontanea, è ciò che dà origine alla radioattività naturale di alcuni elementi chimici: in effetti, solo gli elementi con Z (numero atomico) fino a 82 (Piombo) hanno isotopi stabili.
Superata questa soglia, tutti gli elementi sono soggetti a decadimento. Poiché il numero di protoni è ciò che distingue un elemento da un altro, il decadimento ha anche l'effetto di trasformare l'elemento che decade in un diverso elemento, stabile: praticamente, qualcosa di simile a ciò che cercavano gli antichi alchimisti.
I tempi del decadimento dipendono dall'intrinseca stabilità del nucleo atomico, che a sua volta dipende dal numero di protoni; gli elementi fino al Piombo (Z=82) sono stabili, quelli dal Bismuto (Z=83) fino all'Uranio (Z=92) hanno tempi di decadimento dell'ordine di milioni - in qualche caso miliardi - di anni, poi il processo subisce una brusca accelerazione: gli elementi dal Nettunio (Z=93) fino al Californio (Z=98) decadono in pochi secondi, quelli con un numero di protoni superiore lo fanno in un tempo talmente breve - in genere pochi millisecondi - da non poter esistere in natura.
Secondo i ricercatori, questa caratteristica è ciò che impedisce l'esistenza di nuclei atomici troppo massicci, e molti si spingono fino ad affermare che la Tavola Periodica, così come la conosciamo oggi (con 118 elementi), dovrebbe essere praticamente completa. Non tutti gli scienziati sono però d'accordo, e questa diversità di opinioni ha originato una controversia sulla possibile esistenza di isole di stabilità, cioè sull'esistenza di elementi naturalmente stabili con un elevato numero atomico.

5. QUARK
La scoperta che l'atomo, lungi dall'essere "indivisibile", è in realtà composto da tre elementi (protone, neutrone ed elettrone), ha spinto la ricerca un gradino oltre: è possibile che anche queste particelle subatomiche non siano "elementari" (termine che la fisica moderna utilizza per indicare un elemento indivisibile) ma composte, a loro volta, da mattoni ancora più piccoli?
Ulteriori studi hanno successivamente dimostrato che, mentre l'elettrone è in effetti una particella elementare, questa stessa definizione non si applica a Protoni e Neutroni (riuniti in un'unica categoria, quella degli Adroni, a sua volta suddivisa in Barioni, Mesoni e Barioni Esotici).
Nel 1964, due fisici statunitensi - Murray Gell-Mann e George Zweig - spiegarono alcune incongruenze nel comportamento degli Adroni ipotizzando che non fossero particelle elementari ma complesse, composte da una somma di tre elementi sub-subatomici (o, più semplicemente, quantici) che chiamarono Quark (il nome, secondo quanto raccontato da loro stessi, fu coniato da Gell-Mann in base ad una filastrocca contenuta nel libro Finnegans wake di James Joyce, che stava leggendo in quel periodo: "... three quarks for Muster Mark! / Sure he hasn't got much of a bark / and sure any he has / it's all beside the mark").
Esistono sei differenti tipologie di quark. Benché queste tipologie vengano collettivamente chiamate "sapori", i nomi non sono associati ai sapori (dolce, amaro, salato, ecc...) ma a caratteristiche che hanno colpito i loro scopritori: così, i sei Quark - suddivisi in tre coppie - sono stati chiamati Up e Down (U e D), Charm e Strange (C e S), Top e Bottom (T e B).
Tutti i Quark hanno spin 1/2 e carica elettrica frazionale: +2/3 per Up, Charm e Top, -1/3 per Down, Strange e Bottom.
In natura esistono solo i quark Up e Down, mentre gli altri sapori possono venir creati in scontri particellari ad alta energia, e sono per loro natura altamente instabili.
In natura i quark non esistono come particelle isolate, ma si trovano in gruppi di tre (chiamati Barioni) uniti a formare protoni (UUD, cioè due quark Up e uno Down), neutroni (UDD) o altre particelle esotiche.
Esistono altri tipi di unioni di quark, come i Mesoni (unione di un Quark e di un Antiquark) o i Barioni Esotici (unione di più di tre Quark, come nel Pentaquark).

6. SNARK E BOOJUM
Nel 2272 due fisici teorici di Delta IV - Adhzin Dall e ChitirihRa Payjh - pubblicano un loro studio in cui ipotizzano l'esistenza di particelle subquantiche, che chiamano Snark e Boojum: sarebbero i mattoni elementari che, uniti, costituiscono i Quark. Come nel caso dei Quark, il nome delle nuove "particelle elementari" deriva da un'opera letteraria - in questo caso La caccia allo Snark, di Lewis Carroll.
Nel 2280 la teoria di Dall e Payjh viene - parzialmente - confermata, e gli scienziati autori della sua validazione sperimentale vengono coinvolti nel Progetto Genesis, che però fallisce nel marzo 2282: Snark e Boojum sono stati utilizzati per la creazione della Protomateria, che si rivela una sostanza altamente instabile e pericolosa, con una capacità di rilasciare grandi quantità di energia in modo incontrollato.
Ulteriori studi su Snark e Boojum hanno dimostrato che l'unica possibile configurazione stabile è quella che assumono nei quark, rendendo in questo modo inutilmente dispendioso - in termini di tempo e risorse - ricorrere alla loro creazione in laboratorio e al loro utilizzo, tranne nel caso (vietato dalla Federazione) in cui si vogliano adoperare per la costruzione di armi di distruzione di massa.
Snark e Boojum hanno cariche elettriche che sono il quadrato di quelle dei Quark: 1/9 o 4/9.
Gli Snark sono particelle reali, mentre i Boojum sono il loro equivalente virtuale.
Fonte
MOV 2 "The wrath of Khan / L'ira di Khan"

7. MATERIA E FASI DI AGGREGAZIONE
Secondo la definizione della fisica classica, con il termine Materia si indica "qualsiasi oggetto che abbia una massa e occupi uno spazio".
Questa definizione, che si adatta all'esperienza quotidiana su scala macroscopica, non è però applicabile al mondo della fisica quantistica, sia perché a livello particellare lo "spazio" è prevalentemente vuoto (gli elettroni ruotano ad una distanza dal nucleo che è, mediamente, pari a diecimila volte il diametro del nucleo stesso), sia perché su questa scala le leggi della conservazione della massa vengono spesso violate.
Quando si parla di scala subatomica, quindi, si preferisce utilizzare una diversa definizione: "la materia è composta da Fermioni, una specifica classe di particelle che sono le più piccole entità fisicamente rilevabili".
A prescindere dalla definizione adottata, che dipende dalla scala su cui si lavora, la materia è composta da "mattoni" sempre più piccoli che, in scala decrescente, sono:
- Atomi (nella forma pura, come l'Idrogeno e l'Ossigeno) o molecole (quando gli atomi sono in forma aggregata, come nell'acqua: H2O).
- Gli atomi sono composti da Nucleoni (protoni e neutroni) ed elettroni.
- I Nucleoni sono composti da Quark.
- I Quark sono composti da Snark e Boojum.
A prescindere dalla scala su cui si opera, la materia più trovarsi in differenti Fasi di aggregazione (il termine "Stato" viene considerato impreciso e quindi è stato abbandonato), che dipende da condizioni termodinamiche come temperatura e pressione.
Le sei diverse fasi in cui può trovarsi la materia sono:
Le fasi Solida, Liquida e Gassosa sono le più note, perché sono le uniche che si manifestano su scala macroscopica e in condizioni ambientali standard (ambienti di classe M).
Il Plasma è un gas ionizzato, costituito da un insieme di Ioni positivi e di elettroni liberi.
Nel plasma, la carica elettrica complessiva è nulla (vale a dire che le cariche negative degli elettroni liberi e quelle positive degli ioni si bilanciano).
Il Plasma costituisce circa il 99% della materia osservabile nell'Universo (è la fase in cui si trova la materia nelle stelle e nelle nebulose), sebbene questa stessa "materia osservabile" non costituisca che il 5% circa dello stesso Universo, mentre il restante 95% è dato da materia oscura o energia oscura.
La fase di Superfluido, scoperta nel 1937, è caratterizzata da tre elementi: totale assenza di viscosità, assenza di entropia, conducibilità termica infinita. In sostanza, significa che - a temperature prossime allo zero assoluto - un superfluido è in grado di scorrere all'infinito, senza attrito, realizzando (seppure in condizioni di laboratorio) il "moto perpetuo". La superfluidità riguarda sia i Fermioni che i Bosoni.
La fase di Condensato di Bose-Einstein (ipotizzato nel 1925 dai fisici Satyendranath Bose e Albert Einstein, prodotto sperimentalmente per la prima volta nel 1995 da Eric Cornell e Carl Wiemann dell'Università del Colorado) riguarda i soli Bosoni, che quando vengono portati a temperature prossime allo zero assoluto iniziano a manifestare effetti quantistici su scala macroscopica.

8. ANTIMATERIA
In Fisica - scienza che si è sviluppata a partire dalla chimica - si definisce antimateria la materia costituita da antiparticelle, ovvero particelle che hanno la stessa massa di quelle ordinarie ma carica elettrica opposta.
La tabella sottostante riporta un elenco delle particelle e delle corrispettive antiparticelle, relativamente ad atomi, quark e snark (il numero fra parentesi indica la carica elettrica).
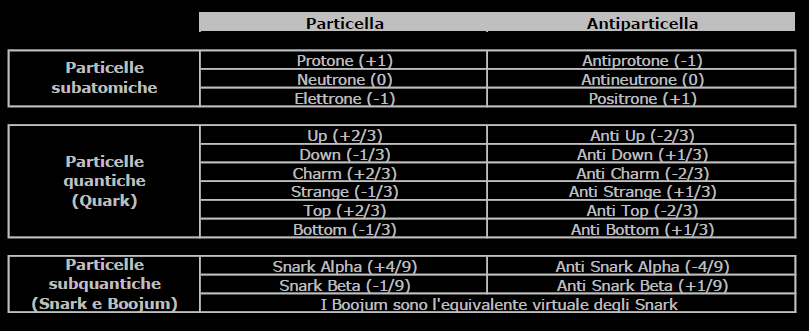
Partendo da questi mattoni fondamentali, è possibile costruire atomi di antimateria corrispondenti ad ogni atomo di materia esistente.
Ad esempio, un atomo di Idrogeno (H) è costituito da un nucleo monoprotonico con un singolo elettrone orbitale, mentre il corrispondente atomo di anti-idrogeno ha un nucleo composto da un singolo antiprotone, con un positrone orbitale a bilanciarne la carica atomica. Il Deuterio (H-2) ha un nucleo composto da un protone e un neutrone, con un elettrone orbitale, mentre l'antideuterio ha un nucleo composto da un antiprotone e un antineutrone, con un positrone orbitale. Lo stesso principio vale per tutti gli elementi e i loro corrispettivi di antimateria.
È utile ricordare che, anche per gli atomi di antimateria, vale il principio della "carica nulla": così come ad ogni protone (+1) deve corrispondere un elettrone (-1), allo stesso modo ad ogni antiprotone (-1) deve corrispondere un positrone (+1).
Come per gli atomi di materia ordinaria, anche per gli atomi di antimateria il numero di neutroni/antineutroni non influenza la carica atomica, perché hanno naturalmente carica nulla. Ciò che li differenzia è il tipo di quark che li compone: UDD (Up, Down, Down, con carica +2/3 -1/3 -1/3 = 0) per il neutrone, -UDD (Anti Up, Anti Down, Anti Down, con carica -2/3 +1/3 +1/3 = 0) per l'antineutrone.
La reazione materia/antimateria (la stessa che alimenta i motori a curvatura delle navi stellari) prende il nome di Annichilazione, ed è il processo più efficiente di produzione di energia che si conosca: entrambe le particelle vengono integralmente convertite in energia. In base al Principio di equivalenza massa/energia, l'annichilazione produce anche particelle: fotoni, elettroni/positroni e perfino nucleoni/antinucleoni.
Un mistero irrisolto della fisica moderna è la quasi totale assenza di antimateria nell'universo osservabile: partendo dall'assunto che il Big Bang abbia creato uguali quantità di entrambe, l'Universo non dovrebbe esistere, perché ogni particella e ogni antiparticella avrebbero dovuto scontrarsi (e continuare a farlo, ogni volta che una coppia di entrambe si forma nel vuoto quantistico) trasformandosi in energia.
Poiché questo non è avvenuto (in fin dei conti siamo qui), e poiché ciò che convenzionalmente chiamiamo "materia" costituisce tutto ciò che osserviamo esistere nell'Universo, alcuni scienziati hanno elaborato una possibile risposta, non ancora verificata sperimentalmente, che presuppone l'esistenza di un universo composto unicamente da ciò che noi chiamiamo antimateria.
La teoria prende avvio dall'osservazione che la Legge di Gravitazione Universale, formulata da Sir Isaac Newton nel 1687, descrive un fenomeno attrattivo sia che entrambe le masse siano positive, sia che entrambe le masse siano negative, mentre se le due masse hanno segno diverso questa legge diventa repulsiva.
Questa osservazione è rimasta classificata come mera curiosità scientifica (in fin dei conti tutte le masse sono positive, nell'ambito della fisica classica) fino a quando non è emersa la famosa equazione di Einstein E=mc2: se la massa è energia, e l'energia può essere negativa (come nell'antimateria), allora può esserlo anche la massa. Ma se due masse con segno opposto si respingono, invece di attrarsi, allora l'antimateria potrebbe non essere stata distrutta nel corso degli istanti successivi al Big Bang, ma essersi "confinata" in un antiuniverso in cui, naturalmente, la nostra antimateria sarebbe l'equivalente della materia, e viceversa.
Questa teoria, se verificata, risolverebbe non uno ma due misteri: dove sia finita l'antimateria (o, meglio: come mai è esistita un'asimmetria fra materia e antimateria che ha permesso la nascita dell'universo, 13.82 miliardi di anni fa), e come mai l'espansione dell'Universo sembra accelerare invece di rallentare, come ci si dovrebbe aspettare da un fenomeno - la Gravitazione Universale - che è attrattivo e non repulsivo.
La repulsione fra universi, definito anche come "antigravità dell'interazione materia/antimateria", spiegherebbe quest'ultimo fenomeno cosmologico senza bisogno di ipotizzare l'esistenza di materia e/o energia oscura.
La produzione di antimateria, in particolare di anti-idrogeno, è prassi operativa standard per la Flotta Stellare, che usa questo anti-elemento (insieme al Deuterio) come combustibile per le reazioni materia/antimateria che avvengono nei nuclei a curvatura delle navi stellari.
Fonte
MAN 2 "TNG Technical Manual"

9. MATERIA ED ENERGIA OSCURA
Secondo le teorie cosmologiche attuali, la Materia Oscura sarebbe una forma di materia che, diversamente da quella conosciuta, non emetterebbe radiazione elettromagnetica e sarebbe, perciò, individuabile solo attraverso i suoi effetti gravitazionali.
L'ipotesi sull'esistenza della materia oscura nasce da un'osservazione: date le emissioni di energia osservabili nell'universo - e le rilevazioni compiute sono abbastanza precise da rientrare nell'errore statistico previsto dalle teorie - e gli effetti gravitazionali prodotti dalla massa derivante da questa energia (per la ben nota equivalenza massa/energia, E = mc2), i conti non tornano, e di un bel po': manca il 95% della massa/energia che dovrebbe esserci.
Il mistero non è di facile soluzione, sia perché - per sua natura - la materia oscura non è rilevabile direttamente, sia perché i ricercatori non sono nemmeno concordi sull'ipotesi della sua esistenza.
Prove certe a questo riguardo non ne esistono, anche se alcune delle prove indirette riguardano l'esistenza delle Galassie (data la loro velocità di rotazione, senza la massa fornita dalla materia oscura dovrebbero disgregarsi), le Lenti Gravitazionali e altri fenomeni di deviazione della luce.
Le teorie sull'esistenza della materia oscura non sono però le uniche a provare a spiegare le anomalie gravimetriche riscontrate. In base al principio logico noto come Rasoio di Occam ("A parità di fattori, è da preferire la spiegazione più semplice"), sono state avanzate spiegazioni che non richiedono l'introduzione di un elemento al tempo stesso così pervasivo e così difficilmente provabile.
Queste ipotesi alternative spaziano da errori nella Legge di Gravitazione Universale, o semplicemente dalla necessità di inserire correttivi in alcune regioni estreme, all'effetto residuo dei buchi neri primordiali, fino alla suaccennata teoria degli effetti prodotti dall'interazione gravitazionale fra materia e antimateria, che avrebbe come corollario un effetto di "compressione" della materia (e, nell'altro universo, dell'antimateria) che potrebbe spiegare le anomalie osservate.
L'Energia Oscura è un altro concetto dibattuto dalla fisica cosmologica: si tratta di una forma di energia che, producendo una massa negativa, avrebbe un effetto di spinta gravitazionale in grado di contrastare la Legge di Gravitazione Universale.
Come nel caso della materia oscura, questa forma di energia non sarebbe rilevabile direttamente ma solo attraverso i suoi effetti, il principale dei quali sarebbe - appunto - l'accelerazione espansionistica dell'Universo.
Gli studi in merito, però, incontrano difficoltà equivalenti: insieme, materia ed energia oscura costituirebbero il 95% dell'universo osservabile (68% di energia e 27% di materia). Nel caso dell'energia, però, essa sarebbe talmente poco "densa", e distribuita in modo così uniforme nel tessuto dello spazio/tempo, da poter rimanere virtualmente irrilevabile anche a livello teorico.

10. TAVOLA PERIODICA DEGLI ELEMENTI
10.1 TAVOLA PERIODICA CLASSICA
La Tavola Periodica degli Elementi (o semplicemente Tavola Periodica), ideata dal chimico russo Dmitrij Ivanovic Mendeleev nel 1869, è lo schema con cui sono ordinati gli elementi chimici sulla base del loro Numero Atomico Z (dal tedesco Zahl, numero), ovvero del numero di protoni presenti nel nucleo di un atomo.
Il lavoro di Mendeleev è ancora più incredibile se si pensa che, nel 1869, si iniziava appena a ipotizzare che l'atomo non fosse indivisibile ma composto da elementi "sub-atomici": le prime ipotesi sull'esistenza dell'elettrone sono del 1860, mentre le prove definitive sono solo del 1911. Anche allora, comunque, si ipotizzava che il nucleo di un atomo fosse un corpo unico, e la scoperta di neutrone e protoni si deve al chimico neozelandese Ernest Rutheford, nel 1920.
Nel 1871 lo stesso Mendeleev pubblicò una forma aggiornata della sua Tavola Periodica, che includeva previsioni sugli elementi secondo lui mancanti, ma che sarebbero dovuti esistere.
Questi vuoti furono riempiti in sequenza quando i chimici scoprirono nuovi elementi reperibili in natura. Inoltre la scoperta dei "gas rari" o "nobili", fra il 1885 e il 1890, fece aggiungere un ottavo gruppo, ovvero una colonna a destra delle sette originariamente indicate da Mendeleev.
In natura si trovano gli elementi con Numero Atomico fino a 92.
Tuttavia, nel 1937, il fisico italiano Emilio Segrè ricrea in laboratorio il Tecnezio, dimostrando così che si potevano creare elementi non esistenti in natura. Il primo di questi, il Nettunio, fu creato già nel 1939. Sebbene, successivamente, siano state trovate tracce naturali di elementi fino al Californio, quasi tutti i cosiddetti "elementi transuranici" hanno tempi di decadenza così rapidi da rendere impossibile il loro studio fuori dai laboratori di ricerca.
Attualmente, la Tavola Periodica comprende 118 elementi. Gli elementi dall'Einsteinio (Es, Z=99) in poi sono chiamati "sintetici", perché possono venire creati solo in laboratorio e non esistono, nemmeno come tracce, in natura.

Tavola Periodica degli Elementi, courtesy of Michael Dayah
10.2 ISOLE DI STABILITÀ
Attualmente, la Tavola Periodica comprende 118 elementi, ma è in atto una controversia in ambito scientifico in merito alla possibile esistenza di elementi stabili, ancorché sintetici, con un peso atomico maggiore.
La maggior parte degli scienziati ritiene che questo non sia possibile perché, come dimostrano tutti gli esperimenti, all'aumentare del numero di protoni aumenta la repulsione elettrostatica, e a un certo punto la forza forte - pur coadiuvata dalla presenza dei neutroni - non è sufficiente a tenere insieme i nuclei atomici. Altri ricercatori, invece, alla luce di alcuni esperimenti - che sembrano dimostrare come nuclei atomici con un elevato numero di nucleoni assumano forme non sferiche - hanno introdotto il concetto di isole di stabilità, ovvero la possibilità che alcuni elementi chimici, pur dotati di numero atomico elevato, sia naturalmente più stabili di elementi con un numero atomico inferiore.
Pur mancando dimostrazioni pratiche - principalmente per la mancanza di strumenti in grado di generare le energie necessarie alla creazione di elementi così pesanti - esistono teorie che identificano tre possibili isole di stabilità, centrate attorno agli elementi 126, 137 e addirittura 155 (il valore si riferisce, naturalmente, al numero di protoni presenti nel nucleo).
10.3 LIMITE DI BOHR
Un ulteriore limite teorico all'ampliamento della Tavola Periodica Classica è dato dallo stato energetico degli elettroni presenti in un atomo.
Al crescere del numero di protoni di un nucleo, infatti, deve corrispondere l'aumento del numero di neutroni, necessari a controbattere la repulsione elettrostatica. L'aumento dei Nucleoni, però, porta ad un aumento del Numero di massa, ovvero all'aumento della massa del nucleo stesso.
Più protoni significa, automaticamente, più elettroni, perché ogni atomo deve avere carica elettrica nulla.
Gli elettroni sono confinati in un Guscio Elettronico, formato da differenti strati, che prende il nome di Configurazione Elettronica ed è soggetto al Principio di Esclusione di Pauli.
In parole povere, ogni strato può ospitare un numero massimo di elettroni, e questi non possono iniziare ad occupare uno strato superiore se quello inferiore non è completamente riempito.
Classicamente, un atomo viene raffigurato come un "Sistema Solare" in miniatura, con il nucleo al posto della stella e gli elettroni al posto dei pianeti. Sebbene questa rappresentazione sia largamente inesatta, in un aspetto l'analogia è corretta: così come i pianeti che si trovano più vicini al Sole devono girargli attorno più velocemente (Moto di Rivoluzione: l'anno di Mercurio è più breve di quello della Terra), analogamente gli elettroni che si trovano più vicini al nucleo devono girare più rapidamente (o, più correttamente: devono possedere più energia).
Il perché, in fisica, è chiaro: ogni massa, che sia una stella come un nucleo atomico, esercita una forza di attrazione (detta Forza Centripeta) che diminuisce secondo la Legge dell'Inverso del Quadrato delle Distanze.
La Forza Centripeta viene contrastata dalla Forza Centrifuga, che spinge l'oggetto orbitante - che sia un pianeta come un elettrone - ad allontanarsi dal centro di massa.
In un sistema equilibrato, le due forze si equivalgono e si raggiunge un equilibrio orbitale.
Ne consegue che, tanto più un corpo orbitale sarà vicino al centro di massa, tanto più velocemente dovrà orbitare. Ma ne consegue anche che, tanto maggiore sarà la massa al centro, tanto maggiore sarà la forza centrifuga richiesta per resistere alla sua attrazione, forza che si manifesta in velocità (o, tecnicamente, in forza vettoriale).
È a questo punto, quindi, che interviene il cosiddetto Limite di Bohr (da Niels Bohr, fisico danese vincitore del Premio Nobel nel 1922).
A differenza dei pianeti, gli elettroni non possono bilanciare parte dell'attrazione allontanandosi dal centro di massa, perché le distanze dei gusci orbitali elettronici sono definite e perché non è possibile riempire un guscio superiore se quello inferiore non è completamente occupato.
L'aumento dei Nucleoni, però, comporta un aumento di massa e gli elettroni, non potendo allontanarsi dal nucleo, possono solo aumentare il loro stato energetico, ossia la loro "velocità orbitale".
Oltre un certo limite di massa (quindi oltre un certo numero di Protoni, tipico degli elementi più pesanti), però, la velocità orbitale degli elettroni dovrebbe eccedere il limite della relatività: in parole povere, gli elettroni degli strati più interni dovrebbero muoversi ad una velocità superiore a quella della luce. E questo, nel continuum quadri-dimensionale, è impossibile.
Niels Bohr ha calcolato che il limite relativistico venga superato per elementi con Numero Atomico superiore a 137, che costituirebbe perciò il limite teorico per una possibile espansione della Tavola Periodica Classica.
10.4 TAVOLA PERIODICA TRANSLUMINALE
Nei primi decenni del XXI secolo, la costruzione di nuovi acceleratori superpotenti (in particolare il Very Large Hadron Collider europeo o il Lunar Linear Accelerator della ECON) ha portato alla scoperta di metodi per rilevare i Tachioni, particelle superluminali previste dalla Teoria della Relatività Ristretta.
Questa scoperta ha prodotto due ricadute nell'ambito della fisica.
Una, senz'altro la più famosa (non foss'altro che per le immense conseguenze che ha avuto), è quella che nel 2033 ha portato il team guidato da un giovane ricercatore dotato di molto talento, Zefram Cochrane, a sperimentare l'accelerazione superluminale, dapprima di elettroni, poi di interi atomi ed infine di corpi complessi, fino al famoso "Primo Balzo" a curvatura il 5 aprile 2063.
La seconda, meno famosa ma non meno importante, è stata la scoperta che esistono elementi chimici parzialmente superluminali.
Se, infatti, il Limite di Bohr resta valido per i normali elementi, la scoperta e validazione sperimentale che è possibile accelerare gli elettroni a velocità superluminale ha aperto ai ricercatori la possibilità di creare elementi stabili con un elevato numero protonico. Di più: la scoperta che non solo gli elettroni, ma anche i Nucleoni possono essere accelerati superluminalmente, ha portato alla creazione di ulteriori elementi sintetici, caratterizzati dall'avere un nucleo in cui una parte di protoni e neutroni sono subluminali e una parte sono superluminali, così come gli elettroni che ne bilanciano la carica.
Fonti
2033: NOV "Federation"
5 aprile 2063: MOV 8 "First Contact / Primo Contatto"
La scoperta degli elementi chimici transluminali (così chiamati perché una parte della loro configurazione è subluminale e una superluminale, e quindi esistono "a cavallo" dei due stati) ha portato alla creazione di una seconda Tavola Periodica, composta da questi nuovi elementi.
Alla fine del XXIV secolo, la Federazione ha identificato un totale di 247 elementi chimici, l'ultimo ad opera della USS Voyager in data stellare 48623 (16 agosto 2371).
Fonti
TAS 1x07 "One of our planet is missing / È scomparso un pianeta"
TNG 6x07 "Rascals / Giovani eroi"
VOY 1x09 "Emanations / Post mortem"
Note
Nell'episodio TAS 1x07 "One of our planet is missing / È scomparso un pianeta", Spock parla di "Elements not known in our periodic tables / Elementi sconosciuti nelle nostre tavole periodiche", evidenziando così che la Federazione ne conosca e utilizzi più di una.
Nell'episodio TNG 6x07 "Rascals / Giovani eroi", gli okudagrammi nella classe scolastica mostrano una Tavola Periodica differente da quella sopra rappresentata, con elementi che nella realtà non esistono (e i cui nomi sono, spesso, giochi di parole od omaggi a personaggi famosi), validando l'affermazione di Spock fatta nella puntata della Serie Animata.
